Воздействие радиочастотно-электромагнитной энергии на все тело может вызвать повреждение ДНК в сперматозоидах мышей по окислительному механизму.
25 ноября 2019 г. Nature.com - Ссылка
(перевод)
Аннотация
Искусственно генерируемая радиочастотно-электромагнитная энергия (RF-EME) теперь повсеместно распространена в нашей среде благодаря использованию мобильных телефонов и устройств связи на основе Wi-Fi. В то время как несколько исследований показали, что RF-EME может вызывать биологический стресс, особенно в контексте мужской репродуктивной системы, механистическая основа этого биофизического взаимодействия остается в значительной степени нерешенной. Чтобы расширить эти исследования, здесь мы подвергали несдерживаемых самцов мышей воздействию RF-EME, генерируемого через специальный волновод (905 МГц, 2,2 Вт / кг) в течение 12 часов в день в течение 1, 3 или 5 недель. В семенниках мышей, подвергшихся воздействию, не было обнаружено явных гистологических изменений или повышенного стресса, независимо от режима воздействия RF-EME. Напротив, 5 недель воздействия RF-EME отрицательно повлияли на профили жизнеспособности и подвижности зрелых эпидидимальных сперматозоидов. Эти сперматозоиды также испытали повышенную выработку в митохондриях активных форм кислорода после 1 недели воздействия, с повышенным окислением и фрагментацией ДНК во все периоды воздействия. Несмотря на эти поражения, воздействие RF-EME не ухудшило способность сперматозоидов к оплодотворению или их способность поддерживать раннее эмбриональное развитие. Это исследование подтверждает полезность мужских половых клеток в качестве чувствительных инструментов для оценки биологических воздействий радиочастотного электромагнитного излучения на все тело. Несмотря на эти поражения, воздействие RF-EME не ухудшило способность сперматозоидов к оплодотворению или их способность поддерживать раннее эмбриональное развитие. Это исследование подтверждает полезность мужских половых клеток в качестве чувствительных инструментов для оценки биологических воздействий радиочастотного электромагнитного излучения на все тело. Несмотря на эти поражения, воздействие RF-EME не ухудшило способность сперматозоидов к оплодотворению или их способность поддерживать раннее эмбриональное развитие. Это исследование подтверждает полезность мужских половых клеток в качестве чувствительных инструментов для оценки биологических воздействий радиочастотного электромагнитного излучения на все тело.
Введение
Благодаря быстрому развитию технологий и росту спроса на электронную связь, использование мобильных телефонов стало практически повсеместным в развитом мире 1 . Мобильные телефоны принимают и излучают радиочастотно-электромагнитную энергию (RF-EME) для передачи информации, и, соответственно, наше воздействие этой формы энергии сейчас беспрецедентно. Таким образом, существует явная необходимость установить правила общественной безопасности при использовании этих мобильных устройств. Однако удовлетворить этот спрос сложно из-за отсутствия понимания того, как RF-EME взаимодействует с биологией. В то время как на сегодняшний день не было обнаружено никаких серьезных клинических эффектов, связанных с воздействием RF-EME 2 , 3 , 4 , 5 , 6., многочисленные исследования показывают, что эта форма энергии может оказывать незначительное пагубное воздействие на биологические системы 7 , 8 , 9 , 10 . Соответственно, Международное агентство по изучению рака еще не отклонило риски RF-EME, вместо этого классифицируя эту форму энергии как потенциальный канцероген. В то время как мы продолжаем обсуждать биологические эффекты хронического воздействия RF-EME, все больше доказательств предполагают, что острое воздействие RF-EME in vitro может вызывать окислительный стресс в ряде модельных клеточных линий 7 , 9 , 11 , 12 , 13. Основная гипотеза, объясняющая механистическую основу этого ответа, заключается в том, что RF-EME нацеливается на митохондрии, что приводит к нарушению потока протонов через внутреннюю мембрану митохондрий и способствует утечке электронов из цепи переноса электронов. Полученное образование супероксидного аниона служит в качестве предшественников для дополнительной генерации активной форм кислорода (ROS), в конечном счете , создает дисбаланс ROS и состояние окислительного стресса.
Потенциал этого механизма биофизического взаимодействия дает толчок для хорошо спланированных исследований, чтобы установить эффект RF-EME после режимов облучения всего тела, которые более точно имитируют воздействие на человека. В этом контексте акцент на мужской репродуктивной системе оправдан из-за обычной практики хранения мобильных телефонов в кармане брюк, помещая их в непосредственной близости от репродуктивного тракта. Дальнейшее подчеркивание актуальности мужской репродуктивной системы свидетельствует о том, что мужские половые клетки особенно восприимчивы к RF-EME 14 и связанному с этим окислительному стрессу 7 , 12.. Действительно, было показано, что сперматозоиды представляют собой чувствительную модель для изучения конкретных физических и химических реакций на RF-EME 15 . Ситуация возникает из-за уникальной архитектуры и метаболизма сперматозоидов, которые делают эти клетки более уязвимыми для повреждения свободными радикалами 16 . Более того, сперматозоиды представляют собой легко поддающиеся оценке средства мониторинга неблагоприятных биологических эффектов с помощью функциональных параметров, таких как подвижность, или более подробного анализа, который может точно определить биохимические нарушения и более тонкие конечные точки, такие как накопление повреждений ДНК. Эти клетки не только служат чувствительной моделью, но и имеют клиническое значение, поскольку индукция повреждения ДНК в мужской зародышевой линии способствует бесплодию 16.и имеет потенциал для распространения в эмбрионе, изменяя траекторию развития и здоровье потомства 16 , 17 .
На сегодняшний день проведено несколько исследований, направленных на оценку воздействия RF-EME на мужскую зародышевую линию. Однако большинство этих исследований сосредоточено на изолированных сперматозоидах или незрелых мужских половых клетках 12 , 15 , 18 , 19 , 20 , 21 . Хотя этот подход способствует изучению сложных биохимических и клеточных реакций на прямое воздействие РЧ-ЭМИ, использование альтернативных моделей грызунов in vivo , вероятно, обеспечит более точное клиническое представление воздействия, что также может способствовать расширению нашего понимания ЭМИ. нарушенные биохимические пути, выявленные in vitroисследования. Модели всего тела предоставляют дополнительное преимущество, так как они позволяют наблюдать целостные эффекты RF-EME на всех стадиях развития мужских половых клеток 22 , включая дифференцировку зародыша в сперматозоиды и их последующее функциональное созревание по мере прохождения ими придатка яичка. Имея устойчивый интерес к установлению биофизических механизмов действия RF-EME на биологию, мы сообщаем об использовании модели на мышах для исследования репродуктивного стресса после режимов воздействия RF-EME на все тело. В частности, специальная волноводная машина (рис. 1 ), аналогичная той, что была разработана Пураненом и его коллегами 23, был разработан, чтобы облегчить воздействие RF-EME на мышей без ограничений на частоте 905 МГц с удельной скоростью поглощения (SAR) 2,2 Вт / кг. Мышей подвергали воздействию RF-EME в течение 12 часов в день, в течение периода от 1 до 5 недель, а затем собирали яички и придатки яичка для исследования влияния RF-EME на сперматогенез и функцию сперматозоидов.
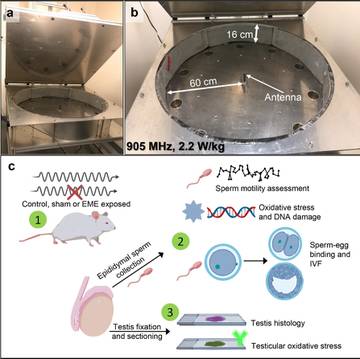
Волноводный прибор, используемый для облучения всего тела RF-EME. Показаны ( а ) полный волноводный аппарат с крышкой в открытой конфигурации и ( б ) крупный план, иллюстрирующий размеры внутренней камеры. ( c ) Графический экспериментальный обзор. (1) Мышей подвергали RF-EME или ложному воздействию в течение 1, 3 или 5 недель и сравнивали с контрольной популяцией, которая не входила в устройство (без лечения). Мышей отбирали, и их сперматозоиды исследовали с использованием функциональных анализов спермы и различных анализов окислительного стресса (2). Семенники этих мышей также исследовали на предмет грубых гистологических аномалий и маркеров окислительного стресса с помощью срезов тканей (3).
....
Воздействие RF-EME на все тело отрицательно влияет на профили жизнеспособности и подвижности зрелых сперматозоидов.
Чтобы изучить влияние воздействия RF-EME in vivo на зрелые сперматозоиды, мы затем исследовали результаты нашего режима облучения на подвижность и жизнеспособность сперматозоидов (рис. 5 ). Было замечено, что общее количество живых сперматозоидов, выделенных из хвостового придатка яичка, уменьшалось при воздействии RF-EME ( p <0,05) (рис. 5a ), эффект, который был особенно очевиден после 5 недель воздействия ( p <0,001); в то время как в популяции, подвергшейся ложному воздействию, никаких изменений не наблюдалось. Аналогичным образом мы отметили значительное снижение процента подвижных сперматозоидов, выделенных от мышей, подвергшихся воздействию RF-EME, после схемы лечения, продлившейся более 5 недель ( p <0,05) (рис. 5b).). Это снижение общей подвижности сперматозоидов происходило соразмерно дефектам объективных измерений прогрессивной и быстрой подвижности сперматозоидов (рис. 5c, d ) у подвергшихся воздействию мышей. В этом отношении влияние на оба параметра снова было наиболее заметным после 5 недель воздействия ( p <0,001). Напротив, сперматозоиды, выделенные из групп фиктивного воздействия, не показали таких изменений в их профиле жизнеспособности или подвижности; при этом оба параметра остаются неотличимыми от тех, которые задокументированы в контрольной группе самцов, не подвергавшейся воздействию.
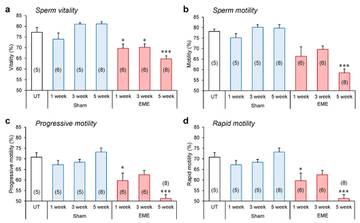
Жизнеспособность и подвижность сперматозоидов снижаются в ответ на воздействие RF-EME. Сперматозоиды собирали из хвостового придатка яичка необработанных контрольных животных (UT), а также из групп имитации и воздействия RF-EME. ( а ) Жизнеспособность сперматозоидов оценивалась методом исключения эозина. Затем с помощью компьютерного анализа спермы определяли процент сперматозоидов, демонстрирующих ( б ) любую форму подвижности, ( в ) прогрессивную подвижность и ( г ) быструю подвижность. Данные представлены как среднее значение + стандартная ошибка среднего (n = 5–8 мышей / группа лечения), при этом анализируется минимум 100 сперматозоидов от каждого животного). Количество использованных биологических повторов обозначено в каждом столбце. * P <0,05, *** P <0,001.
Воздействие RF-EME на все тело повышает окислительный стресс и повреждение ДНК в зрелых сперматозоидах.
Чтобы определить, связаны ли функциональные нарушения подвижности и жизнеспособности сперматозоидов мышей, подвергшихся воздействию RF-EME, с индукцией оксидативного стресса, мы затем исследовали уровни клеточных и митохондриальных АФК, присутствующих в этих клетках (рис. 6 ). В частности, флуоресцентный зонд дигидроэтидия (DHE) был использован для получения информации об уровнях производства клеточных АФК (рис. 6a).). Примерно 14% и 75% сперматозоидов были положительно окрашены на ДГЭ в отрицательной (необработанной) и положительной (т.е. подвергшейся воздействию перекиси водорода) контрольной популяции, соответственно. Когда экспериментальные группы были проанализированы, ни фиктивные, ни условия обработки RF-EME не привели к значительному отклонению от базальной генерации ROS, обнаруженной с помощью DHE-мечения. Это было в отличие от продукции митохондриальных АФК, где зонд MitoSOX Red (MSR) (рис. 6b ) выявил значительное двукратное повышение генерации АФК в митохондриях сперматозоидов животных, подвергшихся воздействию RF-EME в течение 1 или 1 раз. 3 недели по сравнению с контрольными и имитационно экспонированными популяциями клеток ( p <0,05). Интересно, что генерация АФК в митохондриях сперматозоидов нормализовалась до базальных, контрольных уровней после 5 недель воздействия RF-EME.
... вся статья по ссылке
- Подпись автора
Информационный перенос частот веществ, важные ссылки - ПУТЕВОДИТЕЛЬ
Калькуляторы пересчета в частоту высылаю по запросу в личку (после первых результатов)






 Да и с
Да и с 